Sexta-feira, 08 de maio de 2026
Sexta-feira, 08 de maio de 2026
Por Redação O Sul | 5 de maio de 2026
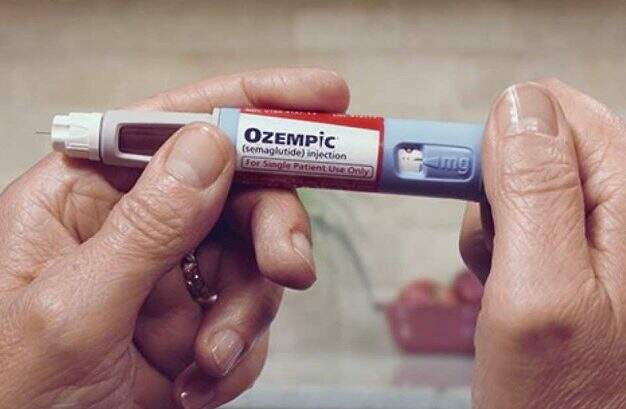
Um levantamento feito pela Anvisa mostra que atualmente oito processos de novos medicamentos à base de semaglutida, princípio ativo do Ozempic, Wegovy e Rybelsus, já estão em análise pela agência. Destes, sete são de origem sintética e um de origem biológica.
Além disso, outros nove produtos aguardam o início da análise pelas áreas técnicas. A agência explica que a análise dos processos atuais teve início no segundo semestre de 2025, após a publicação de um edital que priorizou a avaliação de produtos análogos do GLP-1, que é a classificação da semaglutida.
O primeiro pedido de registro em avaliação entrou na Anvisa no final de 2023, mas a maior parte das solicitações chegou somente no ano passado. A patente da semaglutida no Brasil expira nesta sexta-feira (20), mas para que qualquer medicamento possa ser oferecido no mercado nacional é obrigatória a comprovação de eficácia, segurança e qualidade feita por meio do registro na Anvisa.
Os medicamentos de semaglutida registrados atualmente no país são produtos biológicos. Essa é a classificação de medicamentos elaborados a partir de insumo farmacêutico ativo (IFA) biológico.
São moléculas complexas e podem ser obtidas a partir de fluidos biológicos, tecidos de origem animal ou ainda procedimentos biotecnológicos por meio de manipulação ou inserção de outro material genético (DNA recombinante) ou alteração dos genes. Essa categoria inclui, entre outros, vacinas, soros hiperimunes, hemoderivados e anticorpos monoclonais e canetas GLP-1 feitas por processo biológico.
Esse tipo de medicamento costuma ser aplicado por via injetável (endovenosa ou subcutânea) para garantir a integridade estrutural e funcional das substâncias. Mas também é possível o uso da forma oral.
Já os pedidos de registro em avaliação são de dois tipos: biossimilar, quando é obtido por via biológica, ou sintéticos, quando são obtidos por síntese química – estes últimos são chamados de análogos sintéticos de peptídeos biológicos.
No caso de medicamentos biológicos não existe a opção de registro como genéricos, por isso o produto deve se enquadrar em uma das duas categorias citadas acima. Esses produtos podem ser avaliados a partir de diversos ensaios de comparação com o produto biológico, mas não são genéricos nem similares – são análogos sintéticos de produtos biológicos.
Os análogos sintéticos de biológicos, são obtidos de forma sintética, mas reproduzem a estrutura de um produto biológico. Estes produtos são considerados de alta complexidade, pois possuem características tanto de produtos sintéticos como de biológicos.
A Anvisa esclarece que a avaliação dos análogos sintéticos de semaglutida tem sido tratada com um desafio técnico para as agências reguladoras em todo o mundo. Até o momento nenhuma das principais agências de medicamentos do mundo como as do Japão, Europa e EUA registrou análogos sintéticos da semaglutida.
“Um dos motivos é a necessidade de avaliar estes produtos utilizando parâmetros tanto de fármacos sintéticos como de biológicos. Isso ocorre porque esses produtos compartilham preocupações típicas de medicamentos sintéticos (ex. Resíduos de solventes no processo, resíduos de catalisadores metálicos, impurezas com estrutura química semelhante) quanto as de produtos biológicos (ex. Risco de imunogenicidade, formação de agregados, entre outros)” diz a Agência.
Entre os pontos que merecem atenção técnica estão os ensaios de impurezas, a formação de agregados, a garantia de esterilidade e a imunogenicidade. A avaliação busca garantir, por exemplo, que o medicamento não provoque reações imunes indesejadas, como a criação de anticorpos anti-fármaco, que podem levar à ineficácia de qualquer semaglutida para o paciente, ou mesmo reações de imunidade mais graves. As informações são do jornal O Globo.
Verificação de Email - você receberá um email de confirmação após enviar o seu primeiro comentário, mas ele só será publicado depois que você clicar no link de verificação enviado para a sua conta de e-mail para confirma-lo. Os próximos comentários serão publicados automaticamente por 30 dias!